Combiné AFM / Microscope Optique (BIO-AFM) pour l’imagerie L3 de cellules infectées et pathogènes de classe 3
Echantillons :
Cellules fixées ou vivantes dans leur milieu de culture, bactéries, levures, macromolécules (acides nucléiques, protéines), polymères, fibres, composites, films lipidiques, vésicules lipidiques (GUV, LUV), vésicules extracellulaires (exosomes), structures biologiques purifiées (capsides virales par exemple), bactériophages, « virus-like particles » et virus de classe 2 et 3.
- Taille des plus petits objets détectables en surface: quelques nanomètres X et Y
- Hauteur des objets observables: de 0.5 nm à 12 µm
- Dimension des images carrées: de 50 nm à 100 µm
- Taille des Ă©chantillons observables: 30 mm x 50 mm en X et Y, 5 Ă 10 mm en Z
- Possibilité de travailler en milieu liquide ou à l’air, dans une enceinte thermostatée
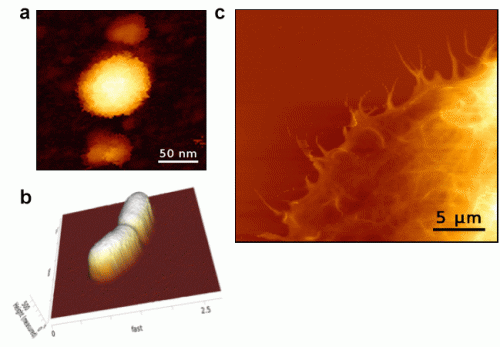
Images AFM :
a) Virus Chikungunya
b) Bacterie
c) Cellule HEK293T
Publications:
Transportin-1 binds to the HIV-1 capsid via a nuclear localization signal and triggers uncoating.
Fernandez J, Machado AK, Lyonnais S, Chamontin C, Gärtner K, Léger T, Henriquet C, Garcia C, Portilho DM, Pugnière M, Chaloin L, Muriaux D, Yamauchi Y, Blaise M, Nisole S, Arhel NJ.
Nat Microbiol. 2019 Oct 14. doi: 10.1038/s41564-019-0575-6.

Figure : In vitro reconstituted HIV-1 proteins using recombinant capsid were contacted with purified Transportin. The images taken by Atomic Force Microscopy illustrate the deformations and breaks by HIV-1 capsid representing (left to right) 10, 20 and 40 min after injection.
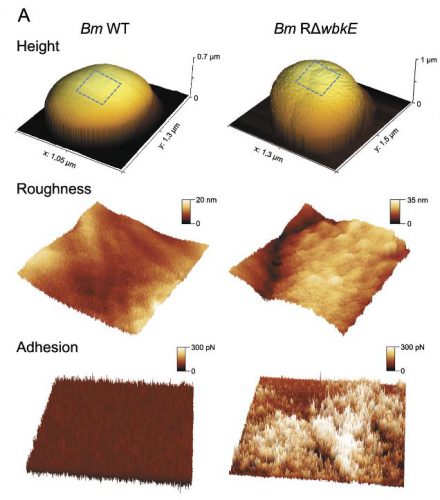
Safia Ouahrani-Bettache, MarĂa P. JimĂ©nez De BagĂĽĂ©s, Jorge De La Garza,Luca Freddi, Juan P. Bueso, SĂ©bastien Lyonnais, Sascha Al Dahouk, Daniela De Biase, StephanKöhler & Alessandra Occhialini. 2019 , Virulence, 10:1, 868-878, DOI:10.1080/21505594.2019.1682762
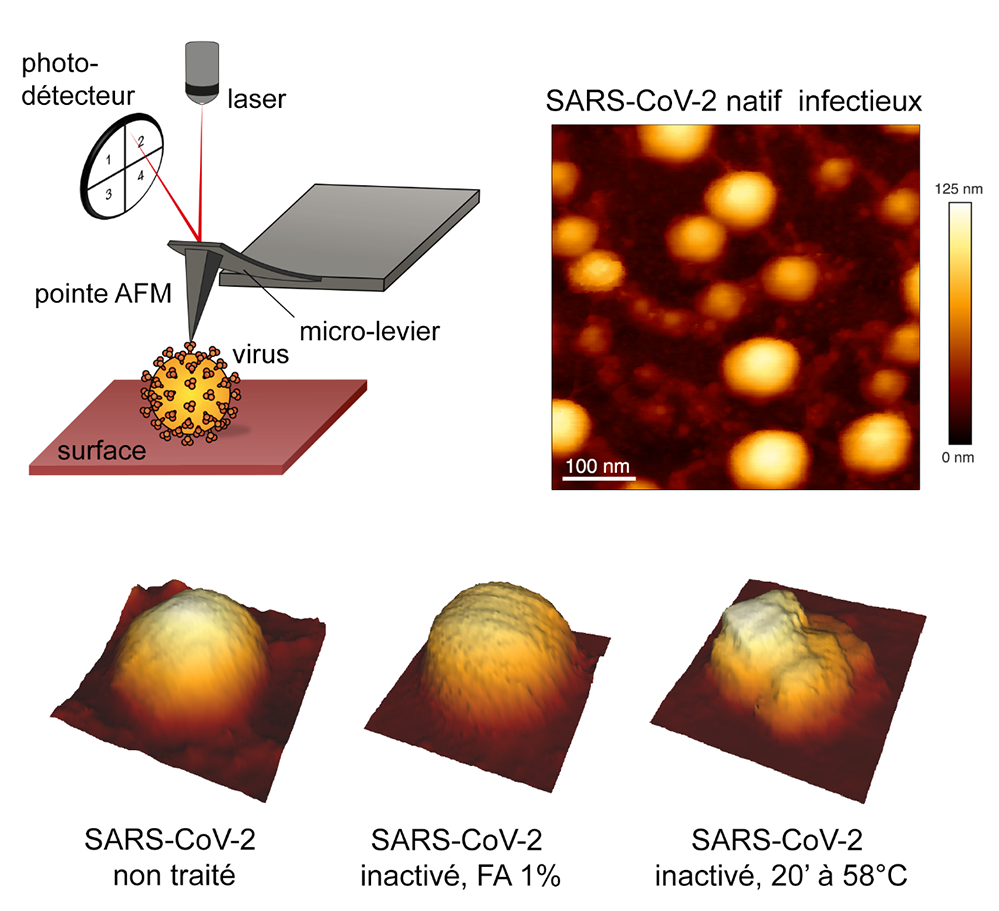
Atomic force microscopy analysis of native infectious and inactivated SARS-CoV-2 virions
SĂ©bastien Lyonnais, Mathilde HĂ©naut, Aymeric Neyret, Peggy Merida, Chantal Cazevieille, Nathalie Gros, Christine Chable-Bessia & Delphine Muriaux. Sci Rep 11, 11885 (2021). https://doi.org/10.1038/s41598-021-91371-4
Ă€ la une de l’INSB

Microscope Optique inversé NIKON Ti2-U avec contraste de phase et fluorescence
Objectifs :
- Nikon CFI Lens Achromat LWD ADL-20x Ph1
- Nikon CFI Achromat LWD ADL-40x Ph2
- NIKON CFI APO VC 100x oil (A.N. 1.4 DT 0.13)
Source LED blanche et Epi-Fluorescence Intensilight 100w (Hg, manuel)
Cubes filtres :
- GFP (Ex466 / 40, DM 495, stop filter BA 525/50)
- mCHERRY, mRFP (Ex562 / 40, DM 593, BA 640/75 stop filter)
- CY5, APC, DiD, Alexa Fluor 647, Alexa fluor 660 (Ex628 / 40, DM 660, BA 692/40 stop filter)
Caméra JENOPTIK Fluorescence ProgRes MFcool (2/3 “1.4 MegaPixel CCD, 1350×1024 pixel resolution, 14bit)



 Chargement en cours ...
Chargement en cours ...